한국원자력연구원 제공
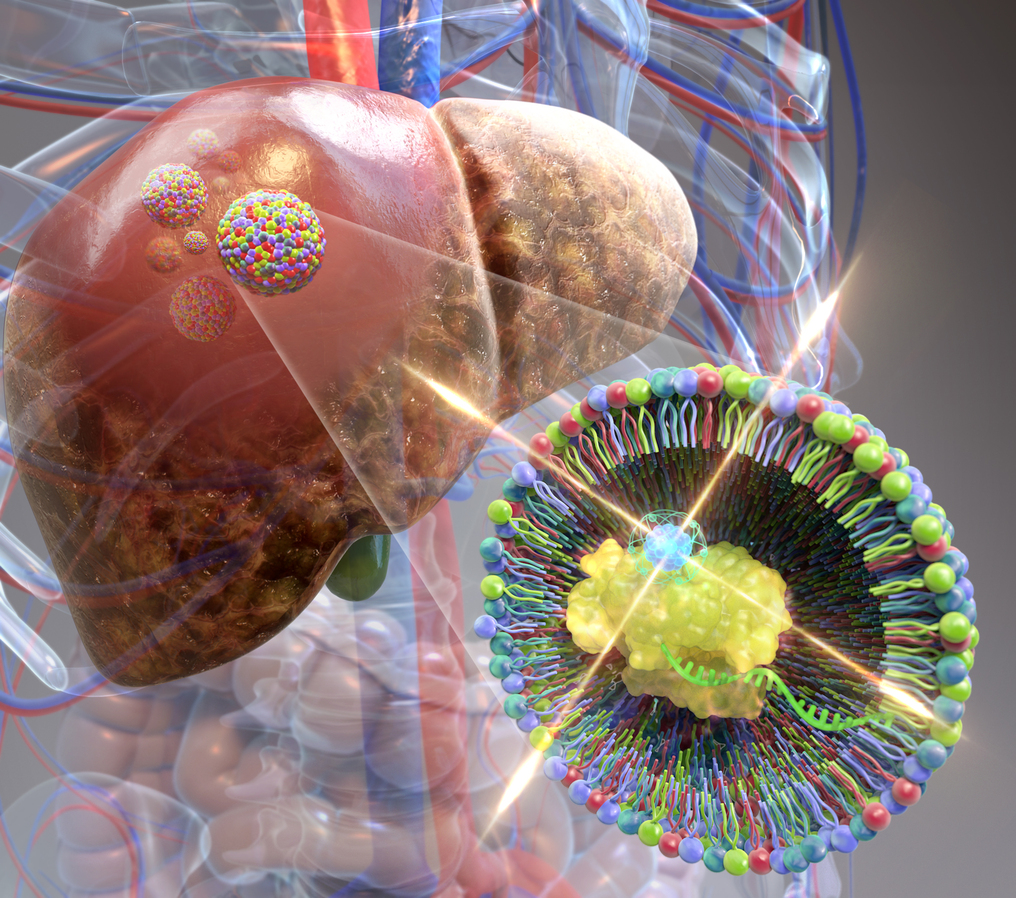
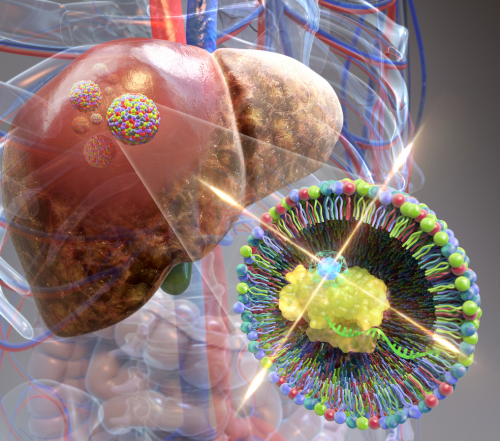
간경화된 부위가 콜라겐 발현 억제 크리스퍼 단백질로 인해 치유가 되는 가상도로 논문 표지 이미지. 연구팀은 크리스퍼 단백질과 지르코늄-89를 합성해 방출되는 감마선에 의해 체내에 있는 유전자 가위 위치를 영상화할 수 있는 기술을 개발해 주목받고 있다.
한국원자력연구원 제공
한국원자력연구원 제공
한국원자력연구원 첨단방사선연구소 가속기동위원소연구실 연구팀은 방사성 동위원소 지르코늄-89(Zr-89)를 이용해 크리스퍼 유전자 가위의 영상화에 성공했다고 23일 밝혔다. 이번 연구 결과는 약물 전달 분야 국제 학술지 ‘저널 오브 컨트롤드 릴리스’ 1월호 표지 논문으로 실렸다.
지난해 12월 미국식품의약국(FDA)은 세계 최초로 크리스퍼 유전자 가위를 치료제로 승인했다. 크리스퍼 유전자 가위는 3세대 유전자 가위로 동식물의 유전자에서 손상된 DNA를 잘라내고 정상 DNA로 교체해 질병을 치료하는 기술이다. 유전자 가위는 길잡이 역할을 하는 가이드 RNA와 표적 부위를 인식하고 잘라내는 효소 단백질로 구성돼 있다.
연구팀은 크리스퍼 유전자 가위 중 하나인 크리스퍼-캐스12a 단백질과 의료용 방사성 동위원소인 지르코늄-89를 접목한 새로운 바이오 소재를 개발했다. 크리스퍼-캐스12a는 크리스퍼-캐스9보다 크기가 작아 더 정교한 유전자 편집이 가능한 기술이다.
유전자 가위는 분자 크기가 크고, 구조가 복잡해 다른 물질과 결합하기 어렵다. 그러나, 연구팀은 의료용 동위원소 지르코늄-89는 반감기가 3.3일로 체내에 오래 머물지 않아 안전하고, 생체 물질 추적이 쉬울 뿐만 아니라 다른 물질과 결합하기 쉽다는 특징에 착안했다.
이에 연구팀은 적절한 배양 온도, 시간 등 최적의 조건을 찾아 유전자 가위 기능을 유지하면서 지르코늄-89와 결합하는 데 성공했다.
연구팀은 간경화 치료를 위해 간경화에 악영향을 주는 콜라겐 증식을 억제하도록 고안된 크리스퍼 유전자 가위를 활용했다. 유전자 가위와 지르코늄-89를 결합한 뒤 체내에서 잘 전달되도록 지질 나노입자로 둘러싸 캡슐화해 정맥주사로 간에 전달했다. 연구팀은 이 과정을 PET(양전자 단층 촬영) 영상으로 확인하면 유전자 가위의 작용 여부를 알 수 있다.
연구팀에 따르면 이번 기술을 활용하면 암과 같은 질환의 진단과 치료가 가능할 뿐만 아니라 약의 이동과 치료 효과를 즉시 파악할 수 있다.
연구를 이끈 박정훈 원자력연구원 가속기동위원소개발실 실장은 “이번에 개발한 소재는 지르코늄-89에서 나오는 감마선을 추적해 유전자 가위가 어디로 이동하는지 영상으로 확인할 수 있는 특징이 있다”라면서 “특정 DNA로 찾아가는 유전자 가위의 정확한 위치를 파악해 치료 효과를 높일 수 있고 신약 연구개발에도 활발히 사용될 수 있을 것으로 기대한다”라고 말했다.
Copyright ⓒ 서울신문. All rights reserved. 무단 전재-재배포, AI 학습 및 활용 금지







































